NEB 发布:GenomONE™ 为诱导 iPSC 形成「保驾护航」
发布人:admin
浏览次数:1433
发布时间:2017-09-20
间充质干细胞(MSC, mesenchymal stem cells)是干细胞家族的重要成员,属于多能干细胞,因其具有多向分化潜能、造血支持和促进干细胞植入、免疫调控和自我复制等特点而日益受到人们的关注。诱导性多能性的间充质干细胞(iPMSCs)是药物筛选、再生医学和细胞治疗的新型候选药物。然而,用于生成骨髓间充质干细胞的诱导性多能性间充质干细胞(iPSC),在导入编码基因的转录因子中,往往伴随有在靶细胞基因组的插入时发生突变的风险。
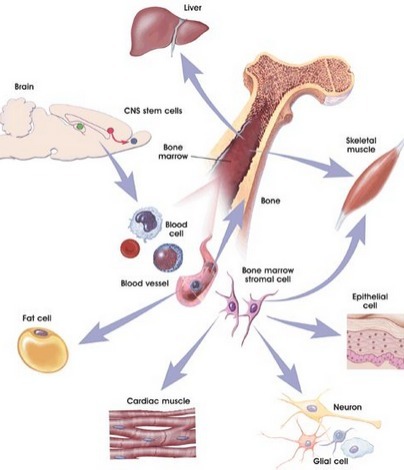
由于近年来对骨髓间充质干细胞认知地深入,在造血系统、免疫系统中的重要作用,怎么样能高效地,精准地利用诱导性多能性间充质干细胞(iPSC)生成骨髓间充质干细胞呢?研究发现使用灭活的病毒颗粒,包装和表达四个纯化重组 Yamanaka 转录因子(Sox2、Oct4,Klf4 和 c-Myc),从而引起人初级成纤维细胞的重编程。全基因组亚硫酸盐测序分析人类 iPMSCs 的全基因组 CpG 甲基化。使用 Western blot、荧光定量 PCR、免疫荧光,和体外分化评估 iPMSCs 的多能性。结果表明这些 iPS 细胞在体外和体内都成功分化成三个胚层的细胞。在本研究中分化诱导后,表达的转录因子被降解,从而改善后续程序分化的效率。由此可见,iPMSC 的重编程和衍生的重组转录因子提供了患者细胞再生医学的一种高效新方法。
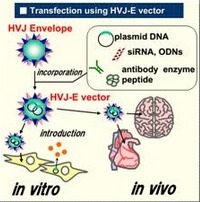
高效新方法的发现,完全归功于灭活的病毒颗粒——仙台病毒包膜。请注意三点:灭活、病毒、包膜。具体来说,灭活使其无毒性,病毒衣壳蛋白的侵染能力,包膜的融合蛋白。也就是这三点作用机制,使得仙台病毒包膜可以高效地,精准地转染细胞,从而完成相关诱导。
(本文转载丁香通)






