在国家自然科学基金(项目编号:81471538,81525012)等资助下,山东大学基础医学院免疫学系高成江教授在抗病毒天然免疫研究领域取得重要进展。相关研究成果分别以“E3 ubiquitin ligase RNF128 promotes innate antiviral immunity through K63-linked ubiquitination of TBK1”(泛素连接酶RNF128通过K63位泛素化修饰TBK1促进抗病毒反应)和“The ubiquitin E3 ligase TRIM31 promotes aggregation and activation of the signaling adaptor MAVS through Lys63-linked polyubiquitination”(泛素连接酶TRIM31通过K63位泛素化修饰促进MAVS多聚体形成及活化)为题于2016年10月24日和12月19日在Nature Immunology上在线发表。两篇论文链接分别为:http://www.nature.com/ni/journal/vaop/ncurrent/full/ni.3588.htm和http://www.nature.com/ni/journal/vaop/ncurrent/full/ni.3641.html。
天然免疫应答是宿主在病原微生物感染后第一时间开启的重要防御措施。宿主细胞在病毒感染后,细胞内的模式识别受体(PRRs)识别病毒的病原相关分子模式(PAMPs),活化复杂的天然免疫信号通路,诱导I型干扰素、促炎性细胞因子和其它一些下游抗病毒效应蛋白的表达,抑制病毒的复制,清除感染机体的病毒。但抗病毒天然免疫信号传导的具体机制尚不清楚。
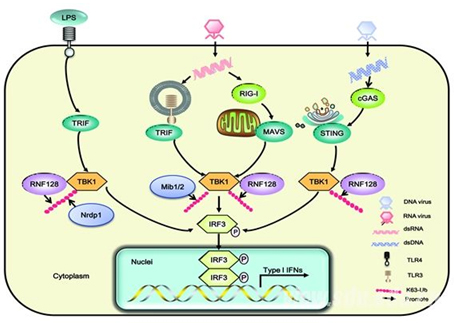
高成江教授课题组发现病毒感染可诱导泛素连接酶RNF128表达;RNF128可通过对抗病毒信号通路中的关键激酶分子TBK1进行K63位泛素化修饰,进而促进TBK1激酶的活化和I型干扰素的分泌,抑制病毒的复制;体内实验进一步证实RNF128缺陷小鼠更易被RNA病毒(VSV)和DNA病毒(HSV-1)所感染。这一研究成果拓展了RNF128在免疫反应调控中的功能,证实RNF128除了在适应性免疫中调控T细胞的功能之外,也能调控RNA病毒和DNA病毒感染所介导的天然免疫信号通路。
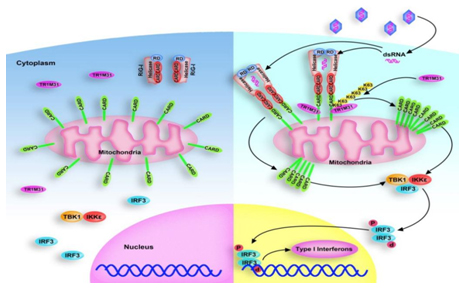
高成江教授课题组还发现RNA病毒感染可诱导泛素连接酶TRIM31募集到线粒体上,并与线粒体上的接头蛋白MAVS发生结合;TRIM31可以对MAVS上第10、311和461位点的赖氨酸进行K63位泛素化修饰,进而增强MAVS多聚体的形成和活化,促进I型干扰素的分泌,抑制病毒的复制;体内实验进一步证实TRIM31缺陷小鼠更易被RNA病毒(VSV或SeV)所感染,而对DNA病毒(HSV-1)的感染没有影响。
上述研究揭示了TRIM31调控RNA病毒介导的天然免疫信号通路的具体机制,发现了TRIM31对MAVS的泛素化修饰是MAVS形成多聚化并活化下游信号通路的重要原因,从而加深了对抗病毒天然免疫信号转导调控机制的了解。
图1 E3泛素连接酶RNF128通过K63位泛素化修饰TBK1促进抗病毒反应
图2 泛素连接酶TRIM31通过K63位泛素化修饰促进MAVS多聚化调控抗RNA病毒免疫反应