

软琼脂克隆形成试验是一种广泛应用于体外细胞转化的技术。
历史上,帕克等人在1956年提出的克隆实验用于评估细胞形成克隆的能力,在这种技术中,细胞被分散到培养板上,生长在饲养细胞或含有必要生长因子的条件培养基上。
这种技术的局限性在于它只提供了关于克隆形成的信息。正常细胞脱离原来生存环境发生一种特定类型的程序化死亡形式,称为失巢凋亡。
然而,转化细胞具有在不与底物结合的情况下生长和分裂的能力。为了利用这一概念,研究人员开发了软琼脂克隆形成试验。近年来,软琼脂克隆形成试验已被改进,以满足特定的需要,一种是掺入荧光染料,允许高通量菌落计数,另一种是使用专门的琼脂溶液,以便在需要蛋白质或DNA样本进行克隆形成后检索活细胞。
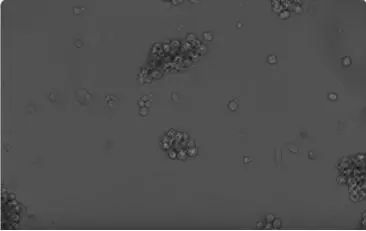
实验操作:
准备材料和试剂:
1、配制2×培养基:1 g培养基粉末,0.2 g碳酸氢钠,加入去离子水,定容到50 mL。
2、将培养基经0.2 μm滤膜过滤除菌。
3、加入目标细胞所需培养基的其他成分。例如:用RPMI 1640培养基培养CMT 167细胞需要加入10% FBS,1% 青霉素/链霉素。使用之前将培养基放在37°C水浴。
4、配制1×培养基,依照目标细胞生长所需培养基配制。
5、配制1%琼脂:1 g琼脂加入到100 mL去离子水中。
6、配制0.6%琼脂:0.6 g琼脂加入到100 mL去离子水中。
7、将配好的琼脂经高温高压灭菌,灭菌后可放在4°C保存,使用前加热至完全溶解。
8、配制氯化硝基四氮唑蓝溶液:1 mg/mL氯化硝基四氮唑蓝加入到1×PBS中。
铺下胶:
1、将熔化的1%琼脂溶液和预热的2×培养基放入装满热水(42°C)的桶(或水浴锅)中,在热水里放一个50 mL的锥形管。将桶放入超净台内。
2、6孔板中的每个孔需要加入1.5 mL混合的琼脂和培养基,为保证足够的量,一个6孔板准备12 mL。
3、首先加入6 mL的培养液到50 mL的锥形管,再加入6 mL的1%琼脂溶液。将锥形管多次翻转混匀,每个孔中迅速加入1.5 mL混合液,加混合液时不能产生气泡。
4、室温静置30 min,待下胶凝固。
铺上胶:
1、收获的细胞用胰蛋白酶消化,用培养基以1:5的比例稀释(如1 mL胰蛋白酶,加4 mL培养基),放入15 mL锥形管。
2、细胞计数:以每孔5000个细胞作为起始,并根据需要进行调整。
3、细胞悬浮液的体积需要1.5 mL。一个6孔板准备12 mL细胞悬液。
4、将熔化的0.6%琼脂溶液放入装有热水(42°C)的桶中,在热水里放一个50 mL的锥形管。将桶放入超净台内。
5、以1:1的比例混合0.6%琼脂溶液和细胞悬液,吸取6 mL细胞悬浮液到50 mL锥形管,再加入6 mL的0.6%琼脂溶液。混匀后迅速加入6孔板中,每孔1.5 ml。小心避免产生气泡。
6、室温静置30 min,待上胶凝固后放入细胞培养箱。
7、足够的菌落形成所需的时间因每个细胞系而异,通常为21天左右。每星期加两次100 g的培养基以防止干燥。